La historia de la fotónica integrada se remonta a finales de la década de 1960, cuando los investigadores de Bell Labs propusieron utilizar técnicas de película delgada para crear estructuras ópticas planas que imitaran el exitoso paradigma de integración de los circuitos electrónicos integrados. El campo ha crecido rápidamente junto con el floreciente campo de las comunicaciones de fibra óptica.
La historia de la fotónica integrada se remonta a finales de la década de 1960, cuando los investigadores de Bell Labs propusieron utilizar técnicas de película delgada para crear estructuras ópticas planas que imitaran el exitoso paradigma de integración de los circuitos electrónicos integrados. El campo ha crecido rápidamente junto con el floreciente campo de las comunicaciones de fibra óptica. Los primeros enfoques de los enlaces de fibra de larga distancia se consideraban fibras llenas de líquido, pero el desafío de guiar la luz a través de materiales de bajo índice de refracción, como gases y líquidos, ha llevado a la óptica integrada. El sistema se implementó principalmente en materiales sólidos. Desafortunadamente, esto ha impedido la creación de dispositivos y sistemas ópticos integrados en campos a gran escala, especialmente en las ciencias de la vida donde los fluidos (aire, agua) son el entorno natural. En los últimos años, los rápidos avances en microfluídica, fotónica de silicio y óptica integrada han convergido en el nuevo y floreciente campo de la optofluídica, que combina la óptica integrada y la fluídica en un solo sistema.
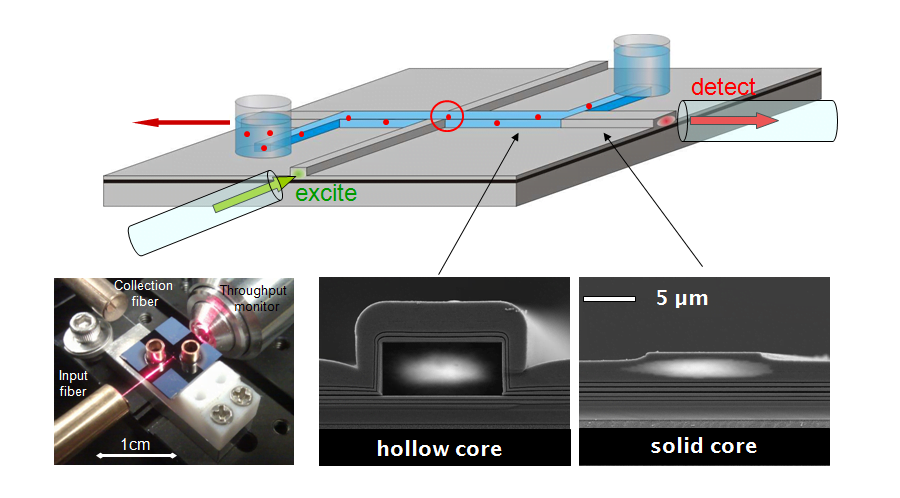
Un grupo dirigido por Holger Schmidt en UC Santa Cruz y Aaron Hawkins en la Universidad Brigham Young ha desarrollado un enfoque único para la optofluídica basado en la creación de canales a escala micrométrica para guiar la luz y los líquidos simultáneamente en un chip de silicio. La combinación de estas ‘guías de ondas de núcleo líquido’ con estructuras de estado sólido convencionales crea un chip plano completamente autónomo, que permite el estudio y la manipulación de fluidos y partículas con la comodidad de los instrumentos de fibra óptica listos para usar. posible. Gran parte de la investigación inicial se centró en investigar las propiedades fotónicas fundamentales, como la propagación óptica de baja pérdida, las estructuras de modo óptico y la implementación del procesamiento de señales ópticas, como el filtrado espectral en guías de ondas de núcleo líquido. Pero el mayor potencial de la tecnología radica en la aplicación de estos dispositivos a áreas históricamente fuera de los límites de la óptica integrada, como la biología molecular, el diagnóstico médico, la toxicología y la espectroscopia de gases. En particular, la demostración de la detección óptica de moléculas fluorescentes individuales mostró la sensibilidad que normalmente se encuentra en equipos de microscopía caros y voluminosos y proporcionó un gran impulso para nuevas investigaciones y aplicaciones relacionadas con partículas individuales en chips.
Con este fin, la Fundación WM Keck ayudó a establecer el Centro de optofluidos a nanoescala en la Universidad de California, Santa Cruz. Dirigido por el profesor Holger Schmidt, el centro incluye cinco departamentos diferentes (H. Noller, Biología Molecular, M. Akeson y D. Deamer, Ingeniería Biomolecular, J. Zhang, Química y W. Dunbar, Ingeniería Informática). En este centro, los investigadores pueden adoptar un enfoque interdisciplinario investigando el uso de elementos a nanoescala en combinación con guías de ondas optofluídicas para abordar problemas de biología molecular, biofísica y diagnóstico médico.
Un área de enfoque de investigación dentro del Centro es la incorporación de nanoporos en dispositivos optofluídicos. El concepto de biofísica de nanoporos reconoció que las moléculas que pasan a través de un orificio a nanoescala en una membrana pueden bloquear parcialmente la abertura, reduciendo la cantidad de corriente eléctrica (iónica) que fluye a través de ese orificio. En efecto, tales estructuras actúan como detectores eléctricos de una sola molécula capaces de distinguir características moleculares al nivel de picoamperios. Recientemente, el profesor Schmidt y el grupo del profesor Noller demostraron la primera detección de ribosomas individuales utilizando nanoporos incrustados en capas dieléctricas que forman guías de ondas optofluídicas de núcleo líquido. Además, al variar el voltaje aplicado, pudimos controlar la cantidad de nanopartículas que ingresan al canal fluídico. Esto abre la posibilidad de utilizar nanoporos como “puertas inteligentes” para introducir partículas fluorescentes individuales en guías de ondas de núcleo líquido donde pueden ser interrogadas “bajo demanda”. Se están realizando colaboraciones adicionales para aplicar este principio al ADN marcado con puntos cuánticos para el análisis genético y la translocación controlada de nanoporos para la secuenciación del ADN.
Otra área de enfoque del Centro es ampliar el tema del control de partículas. El grupo del profesor Schmidt desarrolló recientemente una nueva implementación de captura de partículas ópticas, es decir, el control del movimiento y la posición de las partículas mediante fuerzas ópticas. Usando las propiedades ópticas inherentes de las guías de ondas de núcleo líquido, pudimos retener partículas en posiciones arbitrarias a lo largo del canal fluídico. Además, usamos un haz de luz para acumular más de 100 partículas en un solo punto dentro de la guía de ondas, creando efectivamente el equivalente de un soplador de hojas óptico. Los esfuerzos actuales están dirigidos a crear dispositivos optofluídicos para la clasificación de partículas utilizando fuerzas ópticas para explorar la posibilidad de mover partículas entre nuevos paradigmas de captura y microambientes químicos bien definidos.

La tercera área de enfoque se ocupa de la espectroscopia de una sola molécula para aplicaciones biomédicas. La capacidad demostrada para detectar firmas fluorescentes de moléculas individuales abre la posibilidad de observar y contar biopartículas individuales marcadas, como ácidos nucleicos (ADN, ARN) y proteínas. Desempeñan un papel central en el diagnóstico molecular aplicado a la detección de enfermedades infecciosas, el cribado genético y la medicina personalizada basada en la genómica. La capacidad de discriminar moléculas individuales en una plataforma integrada tiene el potencial de romper el paradigma de diagnóstico actual de amplificar material genómico para crear señales detectables. El grupo de Schmidt está colaborando con varios investigadores clínicos para explorar el potencial de la optofluídica como plataforma de diagnóstico.
Esta instantánea de la investigación realizada en el Centro Keck de la UCSC ofrece una idea del potencial de la optofluídica. Esto abre nuevas ventanas para que los ingenieros ópticos y de dispositivos utilicen las habilidades de ingeniería tradicionales en nuevos contextos que unen a la ingeniería eléctrica con químicos, biólogos, toxicólogos e investigadores médicos. Por lo tanto, este campo emergente proporciona un entorno muy interesante para el desarrollo de nuevas tecnologías ópticas en los años venideros.